肝臟與腸道酯酶在藥物代謝中的關(guān)鍵角色及其與新藥研發(fā)及干細胞技術(shù)的協(xié)同展望
在生物醫(yī)藥領(lǐng)域,藥物在體內(nèi)的代謝過程是新藥研發(fā)與精準(zhǔn)醫(yī)療的核心議題。其中,肝臟和腸道作為關(guān)鍵的代謝場所,其富含的酯酶在藥物轉(zhuǎn)化中扮演著不可或缺的角色。與此人體干細胞技術(shù)的飛速發(fā)展為藥物代謝研究及新藥開發(fā)提供了前所未有的工具與視角。本文將探討肝臟和腸道酯酶在藥物代謝中的作用機制,并闡述其與新藥研發(fā)及干細胞技術(shù)應(yīng)用的緊密聯(lián)系。
一、 肝臟與腸道酯酶:藥物代謝的前沿哨兵
酯酶是一類能夠水解酯鍵的水解酶,廣泛分布于人體各組織,尤其在肝臟和腸道中活性極高。它們是藥物I相代謝(官能團化反應(yīng))的重要參與者。
- 肝臟酯酶的核心地位:肝臟是藥物代謝的“主要化工廠”。肝細胞富含多種酯酶,如羧酸酯酶、膽堿酯酶等。許多口服藥物(尤其是前藥,即本身無活性或活性較低,需在體內(nèi)代謝轉(zhuǎn)化后才發(fā)揮藥效的化合物)經(jīng)腸道吸收后,通過門靜脈首先進入肝臟。肝臟酯酶能迅速水解這些藥物的酯鍵,將其轉(zhuǎn)化為活性形式,或為進一步的II相代謝(結(jié)合反應(yīng))做準(zhǔn)備。這一“首過效應(yīng)”直接決定了藥物的生物利用度和療效強度。例如,抗病毒藥物奧司他韋(達菲)就是典型的前藥,需經(jīng)肝臟酯酶轉(zhuǎn)化為活性代謝物才能發(fā)揮抗流感病毒作用。
- 腸道酯酶的“守門人”作用:腸道不僅是吸收器官,其上皮細胞和腸道菌群也表達豐富的酯酶。藥物在口服后,尚未進入全身循環(huán)之前,便會與腸道酯酶接觸。腸道酯酶代謝可以導(dǎo)致部分藥物在吸收前即被水解失活或激活,顯著影響口服藥物的生物利用度。腸道菌群來源的酯酶其代謝模式可能與宿主酶系不同,增加了藥物反應(yīng)的個體差異性和復(fù)雜性。
作用:肝臟和腸道酯酶共同構(gòu)成了藥物進入體循環(huán)前的雙重代謝屏障與激活站點。它們影響著藥物的起效速度、作用強度、持續(xù)時間以及潛在的毒副作用,是理解藥物個體差異、設(shè)計合理給藥方案的關(guān)鍵。
二、 酯酶研究在新藥研發(fā)中的戰(zhàn)略意義
對肝臟和腸道酯酶機制的深入理解,直接驅(qū)動著新藥研發(fā)策略的創(chuàng)新。
- 前藥設(shè)計:利用酯酶的特異性水解,科學(xué)家可以設(shè)計前藥。這能改善原藥的不良理化性質(zhì)(如溶解性差、口服吸收率低)、提高靶向性、或掩蓋不良味道。設(shè)計時需精確預(yù)測前藥在腸道和肝臟中的代謝速率與路徑,以確保其在正確的位置、以合適的速率釋放活性成分。
- 規(guī)避不良代謝與藥物相互作用:新藥分子若含有易被酯酶水解的基團,需評估其代謝穩(wěn)定性。不穩(wěn)定的藥物可能過早失活,或產(chǎn)生具有毒性的代謝產(chǎn)物。新藥也可能抑制或誘導(dǎo)酯酶的活性,從而影響與其聯(lián)用的其他藥物的代謝,產(chǎn)生復(fù)雜的藥物-藥物相互作用。因此,在臨床前研究中,利用人源肝微粒體、重組酯酶或肝細胞模型進行酯酶代謝穩(wěn)定性及抑制/誘導(dǎo)潛能測試,已成為標(biāo)準(zhǔn)環(huán)節(jié)。
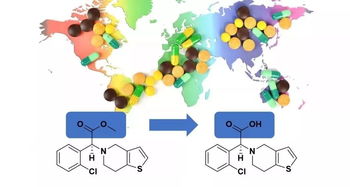
- 個體化用藥的 biomarker:酯酶的活性與表達量存在基因多態(tài)性(如羧酸酯酶1 CES1基因變異),這導(dǎo)致不同人群對某些藥物(如抗血小板藥氯吡格雷的前藥轉(zhuǎn)化)的代謝能力差異巨大。在新藥研發(fā)的臨床階段,對受試者進行相關(guān)酯酶基因型篩查,有助于解釋療效與安全性差異,并為未來的精準(zhǔn)用藥提供依據(jù)。
三、 人體干細胞技術(shù)的革命性賦能
傳統(tǒng)研究多依賴動物模型或永生化細胞系,但這些模型與人體真實的生理和代謝環(huán)境存在差距。人體干細胞技術(shù)的出現(xiàn),特別是誘導(dǎo)多能干細胞(iPSC)和類器官技術(shù),為藥物代謝研究帶來了范式變革。
- 構(gòu)建人源化代謝模型:iPSC技術(shù)可以將個體(包括健康人或特定疾病患者)的體細胞(如皮膚成纖維細胞)重編程為多能干細胞,進而定向分化為功能性的肝細胞樣細胞或腸道上皮細胞。這些細胞能夠表達包括酯酶在內(nèi)的一系列藥物代謝酶,且遺傳背景與供體一致。這為研究酯酶活性個體差異、基因多態(tài)性對藥物代謝的影響,提供了高度人源化、可定制的體外模型。
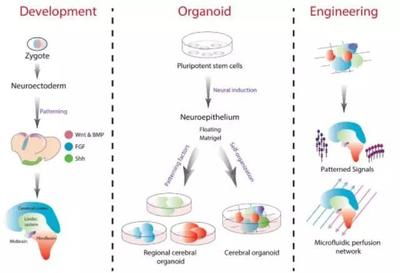
- 創(chuàng)建“肝臟-腸道”互作類器官系統(tǒng):利用干細胞培育的肝類器官和腸類器官,能夠更真實地模擬各自組織的復(fù)雜三維結(jié)構(gòu)和功能。更進一步,科學(xué)家正在嘗試將肝類器官與腸類器官在微流控芯片上共培養(yǎng),構(gòu)建“芯片上的肝-腸”模型。這種系統(tǒng)可以動態(tài)模擬口服藥物經(jīng)腸道吸收、代謝后,通過循環(huán)進入肝臟進行再代謝的完整過程,為研究酯酶在“腸-肝軸”上的級聯(lián)代謝作用提供了前所未有的平臺。
- 加速疾病建模與藥物篩選:從特定遺傳病或代謝性疾病患者衍生出的iPSC-肝/腸細胞,其酯酶功能可能天生異常。利用這些細胞模型,不僅可以深入研究疾病機制,還能高通量篩選針對該代謝環(huán)節(jié)的候選藥物,評估新藥在疾病背景下的代謝特征,實現(xiàn)“從實驗室到臨床”的精準(zhǔn)銜接。
四、 未來展望:整合與精準(zhǔn)
藥物代謝研究將深度融合酯酶生物學(xué)、干細胞技術(shù)與人工智能。通過干細胞模型產(chǎn)生海量的個體特異性代謝數(shù)據(jù),結(jié)合AI進行模擬預(yù)測,我們將能夠:
- 更精準(zhǔn)地預(yù)測新藥在人群中的代謝命運與安全性。
- 設(shè)計更智能的前藥,實現(xiàn)時空可控的靶向釋放。
- 真正實現(xiàn)個體化用藥,根據(jù)患者的酯酶基因型和干細胞模型測試結(jié)果,“量體裁衣”式地選擇藥物和劑量。
肝臟和腸道酯酶是調(diào)控藥物體內(nèi)旅程的關(guān)鍵分子開關(guān)。而人體干細胞技術(shù),正為我們提供一套精準(zhǔn)還原并操控這一過程的強大工具。二者的交叉融合,必將深刻推動新藥研發(fā)從經(jīng)驗驅(qū)動向機理驅(qū)動、從“千人一藥”向“千人千藥”的范式轉(zhuǎn)變,為攻克復(fù)雜疾病和實現(xiàn)精準(zhǔn)醫(yī)療奠定堅實基礎(chǔ)。
如若轉(zhuǎn)載,請注明出處:http://www.eufb.cn/product/56.html
更新時間:2026-04-04 16:45:22